ANTIMICROBIANOS
Un poco de historia
| 1900-15 |
Ehrlich
concibe la idea de usar compuestos químicos de síntesis
como "balas mágicas" selectivas hacia
microorganismos, pero inofensivas para las personas o animales
superiores. En 1909 descubre que el salvarsán es efectivo
contra la sífilis. Acuña el término
"quimioterapia". |
| 1932-35 |
Domagk,
siguiendo los pasos de Ehrlich, descubre la acción del rojo de
prontosilo (la primera sulfamida) sobre el neumococo y otros
estreptococos in vivo. |
| 1940 |
Woods
descubre el mecanismo de acción de las sulfamidas. Estamos en
plena "Edad de oro de la Quimioterapia de síntesis". |
| 1929 |
Fleming
descubre la penicilina, el primer antibiótico natural, pero
fracasa en su intento de purificarlo. La industria farmacéutica
se muestra "indiferente". |
| 1940 |
Chain
y Florey purifican la penicilina. |
| 1944 |
Waksman,
un microbiólogo de suelos, ha iniciado una búsqueda de
microorganismos productores de antibióticos. Descubre la
estreptomicina. Comienza la época dorada de los antibióticos
(quimioterápicos naturales), y la búsqueda racional rinde
decenas de nuevos antimicrobianos procedentes de Actinomicetos,
otras bacterias y hongos. |
Concepto: Sustancia química que impide el
desarrollo o favorece la muerte de un microorganismo.
Los antimicrobianos pueden ser de tres tipos:
-
Desinfectantes: Son sustancias que eliminan la
viabilidad microbiana. Son aplicables sólo a sistemas inanimados.
Ejemplo: hipoclorito de sodio
-
Antisépticos: Son sustancias que reducen y
controlan la presencia de gérmenes potencialmente patógenos.
Aplicables sobre la piel y/o mucosas de humanos y animales. Ejemplo:
Iodopovidona.
-
Antimicrobianos de uso clínico-terapéutico: Son
drogas capaces de reducir y controlar la presencia de gérmenes que
han invadido los tejidos de un individuo.
Existen 2 fármacos de este tipo que nos interesan en
este punto: antibióticos y
quimioterápicos.
Antibiótico: Sustancia que es sintetizada por un
microorganismo vivo. Ej: penicilina
Quimioterápico: Sustancia de preparación sintética.
Ej: Sulfas.
En la práctica se utiliza el término
"antibiótico" para englobar a los antimicrobianos biológicos
(sintetizados por un microorganismo vivo) y
de síntesis. Ambos se caracterizan por poseer "toxicidad selectiva"; no afectan o son
relativamente inocuos para las células del huésped, a diferencia de los
desinfectantes y antisépticos, que afectan a ambos. La toxicidad
selectiva se logra gracias a las diferencias existentes entre el huésped
y el microorganismo invasor; el mejor ejemplo lo constituye la penicilina,
que provoca la lisis bacteriana por inhibición de la síntesis de la
pared celular, no existiendo una estructura comparable en las células de
los mamíferos.
Clasificación de los antimicrobianos

| Según su efecto |
 |
Microbicidas (Bactericidas, Micocidas, etc.)
Microbiostáticos (Bacteriostáticos, etc.) |
| Según su espectro |
 |
Amplio espectro
Espectro limitado
Espectro reducido |
| Según su mecanismo de acción |
 |
Antibióticos que afectan la síntesis de la pared
bacteriana
Antibióticos que afectan la membrana plasmática
Antibióticos que afectan la síntesis proteica procariota
Antibióticos que afectan la síntesis del ADN bacteriano
Antibióticos que inhiben vías metabólicas |
|
 |
CLASIFICACIÓN DE LOS ANTIBIÓTICOS SEGÚN SU
EFECTO |
Efecto bactericida de los antibióticos El
efecto bactericida consiste en producir la muerte del microorganismo
sensible. Los antimicrobianos bacterianos actúan en la fase de
crecimiento logarítmico bacteriano. Los antimicrobianos
bactericidas deben administrarse siempre en infecciones graves, cuando se
necesita la muerte rápida de los microorganismos para controlar la
infección, y cuando no se cuenta con un sistema inmune adecuado para
detener el proceso infeccioso. Ejemplos de enfermedades infecciosas donde
deben utilizarse antimicrobianos bactericidas lo constituyen la
meningoencefalitis purulenta y la endocarditis infecciosa, también se
utilizan en el paciente con
fiebre y neutropenia, o en casos de infección en el paciente con SIDA. Efecto
bacteriostático de los antibióticos El efecto
bacteriostático consiste en producir la inhibición del crecimiento
bacteriano; mientras tanto, se espera que la inmunogénesis aporte los
elementos defensivos necesarios para el control de la enfermedad. Por lo
tanto, estos antimicrobianos no deben indicarse al paciente
inmunocomprometido. Actúan en la fase estacionaria de crecimiento
bacteriano. Algunos antibióticos poseen efecto
bactericida o bacteriostático según la droga actúe in vivo o in
vitro,
y según la dosis administrada. Por ejemplo la Anfotericina B, tiene
efecto fungistático in vivo y fungicida in vitro; la estreptomicina y la
eritromicina tienen efecto bactericida cuando se administran a altas dosis
y efecto bacteriostático si se administran a bajas dosis.
 |
CLASIFICACIÓN DE LOS ANTIBIÓTICOS SEGÚN SU ESPECTRO |
Anbióticos de amplio espectro
Actúan sobre una amplia gama de bacterias grampositivas y
gramnegativas, y también contra Chlamydia, Mycoplasma,
Rickettsia, Espiroquetas y Actinomycetos. Ej: tetraciclinas,
cloramfenicol.
Anbióticos de espectro limitado
Actúan sólo contra cocos grampositivos y gramnegativos,
bacilos grampositivos y espiroquetas. Ejemplo: penicilina.
Anbióticos de espectro reducido
Actúan sólo contra un sector limitado de gérmenes.
 |
CLASIFICACIÓN DE LOS ANTIBIÓTICOS
SEGÚN SU MECANISMO DE ACCIÓN |
Anbióticos que afectan la biosíntesis de la pared
bacteriana
La pared bacteriana es una estructura que protege a la
célula de los cambios osmóticos del medio externo, le confiere forma y
rigidez, y contiene elementos patogénicos característicos de cada especie.
La composición química de la pared celular varía de una
bacteria grampositiva a una gramnegativa. Sabemos que la pared de las
bacterias grampositivas está formada por una capa de 50 a 100 moléculas de
espesor de peptidoglicano, mientras que el peptidoglicano de las bacterias
gramnegativas es sólo de una o dos moléculas de espesor, además de una
capa externa de lipopolisacáridos, que está ausente en las especies
grampositivas. El peptidoglicano está formado por largas cadenas de
polisacáridos en las cuales se alternan en forma lineal N-acetilglucosamina
(NAG) y ácido N-acetilmurámico (NAM). Estas largas cadenas están unidas
en forma cruzada por puentes peptídicos mediante enlaces amida con los
grupos D-alanina del ácido N-acetilmurámico.
La síntesis de la pared bacteriana se ha dividido en 3
etapas:
 |
La primera es intracitoplasmática y consiste en la
síntesis de las unidades NAG y NAM. |
 |
La segunda etapa es intramembranosa; las unidades NAM y NAG
se acoplan mediante un lípido transportador que es el
1-decaprenilfosfato. |
 |
La última etapa es extramembranosa y consiste en la
incorporación del nuevo peptidoglicano al ya existente, es decir se
forman los puentes peptídicos extracitoplasmáticos. |
Los ATB que actúan sobre la pared bacteriana impiden los
sucesivos pasos de la síntesis de la pared bacteriana; como consecuencia
de esta interferencia, la célula bacteriana sin pared no resiste los
cambios osmóticos, se hincha y estalla. Por eso, los ATB beta-lactámicos
(penicilinas, cefalosporinas), bacitracina, vancomicina, teicoplanina y
fosfomicina son bactericidas pues matan a la célula bacteriana en el
momento de la división por lo tanto no actúan cuando la célula está
estática.
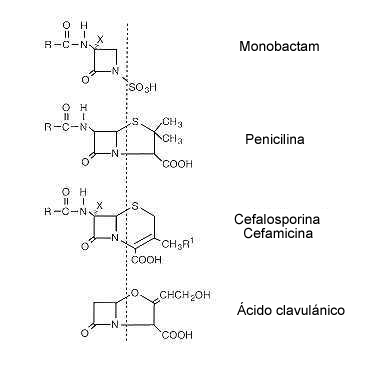 |
| Estructura química de los antibióticos betalactámicos |
Antibióticos que afectan la membrana citoplasmática La
membrana plasmática cumple funciones importantes para la vitalidad de la
bacteria. Entre sus propiedades incluye el actuar como barrera de
permeabilidad selectiva, controlando de esta forma la composición del
medio interno celular. Los antibióticos utilizados en
clínica, que actúan modificando la membrana celular, son las polimixinas y
los polienos (nistatina y anfotericina B) Actúan como detergentes o tensioactivos catiónicos y
provocan una grave alteración de la membrana celular, modificando la
permeabilidad y permitiendo el escape de aminoácidos intracelulares,
purinas, pirimidinas y otras moléculas fundamentales para la vida celular. Las polimixinas
actúan de este modo, interactuando sobre los fosfolípidos de la membrana
celular, mientras que la nistatina y la anfotericina B son activos frente
a hongos, se unen a un grupo
esterol de la membrana que solamente contienen los microorganismos contra
los cuales se utilizan estos ATB.
Las bacterias más susceptibles son las que tienen en su
membrana un mayor contenido de fosfolípidos (gramnegativas). La
insensibilidad o resistencia está en relación con la impermeabilidad de la
pared celular para estos fármacos, como el caso de las grampositivas que
tienen una pared celular muy gruesa. Todos estos
antibióticos son líticos, incluso en bacterias en reposo y tienen cierto
potencial tóxico, especialmente la anfotericina B, ya que son capaces de
unirse con los lípidos de membranas citoplasmáticas de las células de los
mamíferos.
Anfotericina B
Nistatina |
|
|
| IMIDAZOLES |
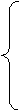 |
Clotrimazol
Miconazol
Ketoconazol
Fluconazol
Itraconazol |
| POLIMIXINAS |
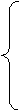 |
Polimixina B
Colistina |
|
Antibióticos que afectan la biosíntesis proteica procariota
Se pueden dividir en dos grupos, según inhiban la
transcripción o la traducción proteica.
-
Inhibición de la transcripción: consiste en la
inhibición de la subunidad beta de la enzima ARN polimerasa ADN
dependiente, que lleva a la inhibición de la síntesis del ARN
mensajero; éste transmite la información del ADN, que es necesaria
para la formación proteica normal.
-
Inhibición de la traducción: se logra mediante la
unión de la molécula del ATB a la subunidad 30S o 50S del
ribosoma bacteriano.
| INHIBICIÓN DE LA TRANSCRIPCIÓN |
|
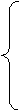 |
Rifampicina
Rifamicina |
|
|
|
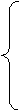 |
TETRACICLINAS |
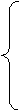 |
Tetraciclina
Oxitetraciclina
Doxiciclina
Minociclina |
|
UNIÓN A LA SUBUNIDAD RIBOSOMAL 30S |
AMINOGLUCÓSIDOS |
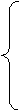 |
Estreptomicina
Neomicina
Kanamicina
Gentamicina
Tobramicina
Amikacina
Netilmicina
Espectinomicina |
| INHIBICIÓN DE LA TRADUCCIÓN |
|
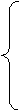 |
Cloramfenicol
Tianfenicol
|
|
|
|
UNIÓN A LA SUBUNIDAD RIBOSOMAL 50S |
MACRÓLIDOS |
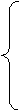 |
Eritromicina
Claritromicina
Roxitromicina
Azitromicina
Espiramicina
Oleandomicina
Miocamicina |
|
|
LINCOSAMINAS |
 |
Clindamicina
Lincomicina |
|
Ver animación de los
distintos mecanismos de acción
Aminoglucósidos: el más estudiado es la
estreptomicina, actuán uniéndose específicamente, de forma irreversible,
con un receptor proteico de los ribosomas 30S. Esta unión causa por una
lado, el bloqueo de la actividad normal del complejo de iniciación, con lo
que se detiene la síntesis proteica y, por otro, distorsiona el codón del
lugar A, provocando la incorporación del ARNt a un aminoácido distinto al
codificado, formándose proteínas anómalas.
Tetraciclinas: se unen a los ribosomas 30S y
bloquean la fijación del aminoacil-ARNt en el lugar A.
Cloramfenicol y lincosamidas: se unen en el
ribosoma 50S e impiden la transferencia, inhiben la peptidiltransferasa y,
por ello, la transpeptidación..
Macrólidos: actúan sobre los ribosomas 50S, impidiendo la translocación, es decir, el paso del peptidil-ARNt del lugar A al P,
previa liberación del ARNt
Antibióticos que afectan la síntesis de ácidos nucleicos
bacterianos
La biosíntesis del ADN bacteriano es inhibida por dos
mecanismos:
-
Mediante la inhibición de una topoisomerasa, llamada ADN
girasa, enzima
esencial para la replicación del ADN. La ADN
girasa posee dos subunidades, A y B; la subunidad B cumple la función
de enrollar las cadenas de ADN, paso necesario para acomodar el
núcleo dentro de la bacteria mediante la reducción de su tamaño.
Cuando este superenrollado ha finalizado, la subunidad A sella el
corte en el ADN. Por ejemplo: las quinolonas inhiben la actividad de esta enzima.
-
Mediante la formación de compuestos tóxicos para las
bacterias, resultante del poder reductor de los anaerobios
sobre el radical "nitro" de los ATB nitroimidazólicos. Los
productos de reducción del grupo "nitro" se conjugan con el
ADN, produciendo su desestabilización y por lo tanto provocando la
muerte celular.
| NITROIMIDAZOLES |
 |
Metronidazol
Ornidazol
Tinidazol
Secnidazol |
Griseofulvina
5Fluorocitosina |
|
|
|
Antibióticos que inhiben vías metabólicas
(quimioterápicos)
Ciertos ATB, como las sulfamidas y la trimetoprima,
inhiben vías metabólicas que impiden el crecimiento bacteriano; tienen
por lo tanto acción bacteriostática. Cuando ambas drogas se administran
en forma conjunta, su acción es bactericida.
Las sulfamidas inhiben competitivamente la incorporación
de ácido paraaminobenzoico (PABA) por su semejanza química, impidiendo a
partir de este precursor, la síntesis de ácido fólico bacteriano,
factor esencial en el crecimiento de los microorganismos. Cuando la
bacteria adquiere la capacidad de producir PABA o de inhibir las
sulfamidas, se transforma en resistente.

 |
|
Estructuras químicas de algunas sulfas |
La trimetoprima (TMP) inhibe a la dihidrofolato
reductasa (enzima reductora del
ácido dihidrofólico, con lo cual obstruye la
formación de ácido tetrahidrofólico, metabolito esencial para la
síntesis de purinas por la bacteria. La enzima de la bacteria es 50.000 a
100.000 veces más sensible a la TMP que la enzima humana, con lo cual se
explica su acción. El ser humano no sintetiza ácido fólico sino que lo
incorpora con su dieta, por lo tanto la TMP no afecta la síntesis de
purinas en el hombre. El bloqueo secuencial de la misma vía bioquímica
por las sulfamidas y la TMP resulta en un alto grado de sinergismo contra
un amplio espectro de microorganismos.
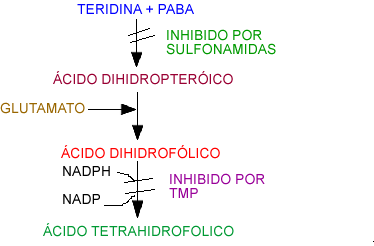 |
|
Esquema
de la síntesis del ácido fólico
|
| ANÁLOGOS DE METABOLITOS BACTERIANOS |
 |
SULFAMIDAS |
 |
Sulfametoxazol
Sulfadiazina
Sulfisoxazol
Sulfametoxidiazina
Sulfametoxipirazina |
| INHIBIDORES DE ENZIMAS BACTERIANAS |
 |
Trimetoprima |
|
|
|
Existen 3 categorías de los efectos in vitro debidos a las
interacciones entre antimicrobianos.
-
Sinergismo: cuando la actividad debida a los
antimicrobianos en combinación, es mayor que la suma de los efectos
individuales de cada uno de ellos.
-
Antagonismo: disminución de la actividad de un fármaco
en presencia de otro.
-
Indiferencia o Adición: cuando la acción combinada de 2
antimicrobianos no produce un efecto mayor que el predecible por las
actividades individuales de cada droga.
Los antimicrobianos ejercen fuertes presiones selectivas
sobre las poblaciones bacterianas y favorecen a aquellos microorganismos
que son capaces de resistirlas.
Aclaraciones de nomenclatura:
Cepa insensible: es aquella cuyo fenotipo silvestre
le permite "resistir" de modo natural a un determinado
antibiótico. La base de esta insensibilidad suele ser alguna estructura
de la bacteria que actúa como barrera (como por
ejemplo, la membrana externa de Gram-negativas, que dificulta el paso de
muchoa agentes antibacterianos).
Cepa resistente: es una variante surgida por
cambios genéticos a partir de un fenotipo silvestre originalmente
sensible.
Resistencia natural
Es la que ofrecen las bacterias de una misma especie o
cepa frente a un determinado antibiótico; todos los integrantes de la misma
especie son resistentes al fármaco. Ej: Pseudomonas aeruginosa,
naturalmente resistente a las cefalosporinas. Son cepas insensibles.
Resistencia adquirida
Esta resistencia afecta a algunas bacterias de una misma
especie o cepa pero no a la totalidad; se logra en el transcurso del
tiempo por dos mecanismos básicos: por mutación en un gen
cromosómico
(resistencia cromosómica) o por la adquisición de material genético
extracromosómico -plásmidos- (resistencia extracromosómica).
-
Resistencia cromosómica: se origina por mutación
espontánea, hecho que lleva a un cambio genético estable. En una
primera etapa aparecen pocas bacterias resistentes, pero a medida que
el antibiótico selecciona los microorganismos, se desarrollan células
resistentes hasta transformarse en un cultivo puro antibiótico-resistente. La
mutación espontánea puede acelerarse por acción de agentes físicos
mutágenos o sustancias químicas. Por ejemplo: Pseudomonas
aeruginosa frente a aminoglucósidos.
-
Resistencia extracromosómica: se produce por
incorporación de material genético por fuera del cromosoma
bacteriano. Se la llama también resistencia transferida o resistencia
mediada por plásmidos o transposones. El rápido aumento de la
diseminación de la resistencia de un antibiótico dentro de una misma especie
o entre especies está relacionado con la diseminación de plásmidos
de resistencia. Los transposones son segmentos de ADN que se pueden
trasladar desde una a otra zona del cromosoma bacteriano o entre el
cromosoma y un plásmido o entre el cromosoma y el ADN de un bacteriófago; la
transposición es un proceso siempre presente en las poblaciones
bacterianas. El ingreso del material transferido puede realizarse por
diferentes mecanismos denominados:
-
Conjugación: consiste en la transferencia de genes
entre bacterias sexualmente diferentes; requiere del contacto de
célula a célula a través de pelos sexuales para la transmisión del
factor R (gen extracromosómico de la resistencia). Hay un puente
citoplasmático de conjugación entre bacterias de distintas especies.
La resistencia así obtenida se extiende con rapidez, pues cada
bacteria infectada se transforma en donante de genes de resistencia.
Ver animación en http://www.biologia.edu.ar/animaciones/index.htm
-
Transducción: se realiza por medio de bacteriófagos,
que transportan ADN de una bacteria a la otra. Ver animación en
http://www.biologia.edu.ar/animaciones/index.htm
-
Transformación: se produce entre bacterias
homólogas; al producirse la lisis de una bacteria resistente, una
porción de ADN penetra la pared celular de una bacteria susceptible y
ambos ADN se combinan.
-
Transposición: consiste en el intercambio entre
plásmidos, o de un plásmido hacia un cromosoma o hacia un
bacteriófago sin necesidad de homología entre el donante y el
receptor. Los elementos así actuantes son los denominados
transposones, que seleccionan su propio sitio de inserción.
-
Inactivación enzimática del ATB: la
resistencia a los ATB beta-lactámicos se debe principalmente a la
producción de betalactamasas, enzimas bacterianas que rompen la
unión amida del ciclo betalactámico. Existen numerosas
betalactamasas, codificadas por genes cromosómicos o por genes
transferibles localizados en plásmidos o transposones. Se han
definido tres clases de betalactamasas: las de clase A, B y C.
La resistencia a aminoglucósidos se debe a enzimas
codificadas por genes localizados en plásmidos o en el cromosoma; varias
de estas enzimas son transportadas en transposones. Dichas enzimas pueden
inducir N-acetilación, O-nucleotidilación y O-fosforilación.
La cloramfenicol acetiltransferasa (CAT) es producida por
bacterias grampositivas y gramnegativas. Esta enzima intracelular inactiva
el antibiótico transformándolo en su deriva y está codificada por genes localizados en el
cromosoma bacteriano o en plásmidos.
Recientemente se ha aislado de Escherichia coli una
enzima denominada eritromicina estearasa, que inactiva el ciclo lactona de
la eritromicina.
-
Disminución de la permeabilidad celular hacia
el ATB: El pasaje
de los antibiótico hidrófilos a través de la pared celular está facilitado
por la presencia de porinas, proteínas que forman canales de
difusión llenos de agua que pueden ser atravesados por los
antibiótico. Las
bacterias producen un número elevado de porinas y regulan el número
de las mismas. Cuanto más grande es la molécula del antibiótico, mayor será
el número de cargas negativas y por lo tanto más elevado el grado de
hidrofobicidad; por ejemplo las pequeñas moléculas hidrófilas
del imipenem, cruzan fácilmente la pared, mientras que moléculas
con carga mucho mayor, como la carbenicilina (una penicilina de amplio
espectro), la atraviesan en menor
grado.
Alteración del mecanismo de transporte del antibiótico: cuando el
antibiótico accede al interior bacteriano por algún mecanismo de transporte
específico, una mutación que afecte a dicho sistema de transporte
supondrá una mayor resistencia al antibiótico. Por ejemplo en E. coli la
cicloserina entra aprovechando el sistema de transporte de la valina o la
glicocola. Determinados mutantes incapaces de transportar estos
aminoácidos son resistentes a la cicloserina.
-
Producción de flujo de ATB a través de la membrana
celular: es debido a la presencia de proteínas de membrana
especializadas. Se altera la producción de energía y se disminuye no
solamente la entrada del antibiótico sino que a su vez las bacterias
reducen la concentración del antibiótico y se promueve la extracción
activa del mismo. Tal mecanismo de resistencia ha sido demostrado para la tetraciclina en los bacilos gramnegativos y recientemente en Escherichia
coli para la eliminación de fluoroquinolonas.
-
Alteración de los sitios de ataques ribosomales: la
falta de unión del antibiótico a su receptor "blanco" en el
ribosoma, anula su capacidad para inhibir la síntesis de proteínas y
el crecimiento celular. Esta resistencia se produce como resultado de
la acción de una metilasa, que demetila los residuos de adenina en el
ARN ribosomal 23S de la subunidad 50S, que interfiere con la fijación
de la estreptomicina al ribosoma.
-
Síntesis de una nueva enzima resistente: algunas
bacterias con resistencia mediada por plásmidos, elaboran enzimas
evasivas que eluden el bloqueo metabólico efectuado por sulfamidas o
TMP mediante distintos poros secuenciales; por ejemplo pueden
reemplazar a la enzima dihidrofolatoreductasa, sensible a estas
drogas, por otra enzima 20.000 veces menos susceptible a la
inhibición. Las bacterias gramnegativas resisten a las quinolonas
alterando la ADN girasa.
-
Aparición de otra vía metabólica alternativa: las
bacterias pueden adoptar otras vías metabólicas para obtener el
sustrato necesario para sus requerimientos vitales; por ejemplo,
pueden utilizar tiamina o metionina en lugar de ácido
paraaminobenzoico (PABA) para la síntesis de ácido fólico y así
hacerse resistentes a la TMP-Sulfametoxazol.
Resistencia cruzada Abarca a los
antibióticos de estructura química idéntica; cuando el microorganismo adquiere
resistencia a un determinado antibiótico, también será resistente a los
demás integrantes de ese grupo de fármacos. Tal es el caso de
Bacteroides para los aminoglucósidos o Staphylococcus para
tetraciclinas. El conocimiento de la resistencia cruzada evita la
prescripción de antibióticos similares cuando fracasa la terapéutica.
ANTIBIOGRAMA

Introducción
También conocidas como antibioticogramas o pruebas de
susceptibilidad in vitro a los antibióticos . Son métodos de
laboratorio que estudian la sensibilidad de un microorganismo a la acción
de los antibióticos. El término sensible es muy usado como sinónimo de
susceptible. Susceptible significa que un microorganismo es inhibido o
muerto en las pruebas in vitro por una concentración del
antibiótico accesible en
la sangre, cuando ese mismo antibiótico se usa in vivo.
Estas pruebas pueden ser de tipo cualitativo si el
resultado expresa la característica de susceptibilidad o resistencia de
un microorganismo frente a un antibiótico; o de tipo cuantitativo si permite
obtener información gradual de esa susceptibilidad.
Para establecer el tratamiento correcto de cualquier
infección bacteriana debemos apoyarnos, siempre que sea posible, en el
conocimiento del agente etiológico y el conocimiento de la sensibilidad
de dicho agente a los antibióticos.
Se debe solicitar un antibiograma cuando:
-
El microorganismo aislado, causante de la patología,
no es uniforme en su comportamiento frente a los antibióticos usuales.
-
En infecciones microbianas graves que comprometen
seriamente la salud del paciente. Ej: endocarditis, absceso cerebral,
septicemias, osteomielitis, meningitis, etc.
-
Si se desconoce la susceptibilidad del microorganismo
aislado a los antibióticos de uso frecuente.
-
En una patología que no responde al tratamiento
antibacteriano clásico.
Pruebas de susceptibilidad
Se clasifican en:
 |
Pruebas cuantitativas |
 |
Pruebas cualitativas |
 |
Pruebas especiales: |
-
Pruebas de Beta-lactamasa
-
Poder inhibitorio del suero
-
Poder bactericida del suero
-
Interacción sinérgica de los ATM
Pruebas cuantitativas
Antibiograma por dilución: permiten cuantificar
hasta que grado un microorganismo es susceptible a la acción de un ATM.
Puede realizarse en medio líquido o sólido. Permite conocer la
concentración inhibitoria mínima (CIM) de un ATM necesaria para inhibir
el desarrollo de un microorganismo
Pruebas cualitativas
Antibiograma por difusión: hay distintas
técnicas, la de mayor utilización es el método de Kirby- Bauer, que
trabaja con medio de cultivo sólido en placa de Petri y discos de ATM. Si
el microorganismo en estudio es susceptible a la acción del ATM, se
formará un halo de inhibición alrededor del disco, luego de haber
incubados las placas a temperatura y tiempo adecuados.
Pruebas especiales
-
Pruebas de betalactamasas: permite detectar la
producción de dichas enzimas por diferentes especies bacterianas.
Varias pruebas pueden utilizarse para conocer la producción de
betalactamasa bacteriana. Las más utilizadas son:
 |
Método rápido yodométrico |
 |
Método acidométrico |
Estos métodos deben usarse con cultivos puros de
bacterias y no con secreciones humanas (o sea muestras).
La principal ventaja de estos métodos es la rapidez de su
realización, la certeza de sus resultados si se tiene la cepa patógena
aislada y su fácil lectura.
-
Poder inhibitorio del suero: permite determinar la
actividad antibacteriana en el suero del paciente durante la terapéutica
antimicrobiana para poder evaluar la eficacia de la dosis de
antibiótico que
está recibiendo. Su aplicación está limitada a patologías graves
en inmunodeprimidos, en casos de trastornos en la absorción,
metabolismo y/o excreción del antibiótico y en control de tratamientos
prolongados.
-
Interacción sinérgica de los antibióticos:
consiste en colocar en una serie de tubos cantidades constantes de una
dilución cuatro veces menor que la CBM de una droga en combinación
con concentraciones de la segunda droga desde la CBM hasta un octavo o
menos, manteniendo una concentración constante del inóculo
bacteriano.
(CIM)
Concentración
inhibitoria mínima: Es la concentración del antibiótico
requerida para impedir el crecimiento bacteriano a partir de la incubación
de 10 5-6 bacterias en fase de crecimiento rápido, en un medio
libre de proteínas con pH 7,2, aerobio, durante un periodo de incubación
de una noche.
Este término es importante porque se utiliza para determinar la
sensibilidad bacteriana a un agente antibiótico específico. Es
importante recordar que las condiciones in vivo son distintas a las
utilizadas para esta prueba que se realiza in vitro.
En un ser vivo la bacteria generalmente se encuentra un medio más ácido
y anaerobio. Además es mayor tamaño del inoculo bacteriano y
probablemente no está en fase rápida de crecimiento; lo cual disminuye
el valor predictivo del CIM.

"Fluoroquinolonas,
Sulfonamidas, Trimetoprim y Antisépticos Urinarios."
http://med.javeriana.edu.co/fisiologia/fw/c76.htm
Antimicrobianos
http://www.qb.fcen.uba.ar/microinmuno/SeminarioAntibioticos2.htm

 |
Basualdo Juan A.; Coto, Celia; de Torres Ramón
A.(1996). Microbiología Biomédica.
|
|