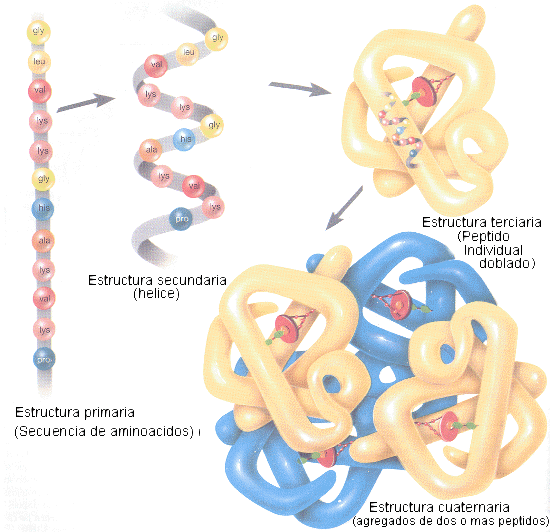Proteínas: de la estructura primaria a la cuaternaria

Estructura de las Proteínas|Polipéptidos|Estructura
primaria |Estructura secundaria|Estructura Terciaria|Estructura cuaternaria|
Enlaces | Glosario

[ Principal ] [ Arriba ] [ Estructura de la Materia ] [ Biomoléculas ] [ Lípidos ] [ Azucares ] [ ADN ] [ ARN ] [ Aminoácidos ] [ Estructura protéica ] [ Proteínas ] [ Fosfolipido ]

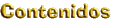

 Esta es una molécula
de hexoquinasa, una proteína del metabolismo que se encuentra en
la mayoría de los seres vivos. Esta compuesta por aproximadamente
6000 átomos y pesa 40 kiloDaltons, también tiene una molécula
de glucosa pegada que no se representa en el esquema. Esta es una molécula
de hexoquinasa, una proteína del metabolismo que se encuentra en
la mayoría de los seres vivos. Esta compuesta por aproximadamente
6000 átomos y pesa 40 kiloDaltons, también tiene una molécula
de glucosa pegada que no se representa en el esquema.
A primera vista podría pensarse en las proteínas como polímeros
lineales de aminoácidos unidos entre sí por medio de enlaces peptídicos. Sin
embargo, la secuencia lineal de aminoácidos puede adoptar múltiples
conformaciones en el espacio.
Las uniones peptídicas se establecen entre los grupos amino y los
carboxilo de otro aminoácidos, formando dipéptidos--> tripéptidos-->
tetrapéptidos--> POLIPÉPTIDOS. Cada enlace forma un plano
Algunos polipéptidos funcionan per se como hormonas (Insulina y glucagón -->> regulan la glucosa en sangre) o neurotransmisores
(colecistoquinina--> sensación de hambre)
La estructura primaria viene
determinada por la secuencia de aminoácidos en la cadena proteica, es decir, el
número de aminoácidos presentes y el orden en que están enlazados. La conformación
espacial de una proteína se analiza en términos de estructura
secundaria y estructura terciaria. La asociación de varias
cadenas polipeptídicas origina un nivel superior de organización, la
llamada estructura cuaternaria.
Por último, la asociación de
proteínas con otros tipos de biomoléculas
para formar asociaciones
supramoleculares con carácter permanente da lugar a la estructura
quinaria.
Las proteínas tiene múltiple niveles de estructura. La básica
es la estructura primaria.
La estructura primaria de una proteína es simplemente el
orden de sus aminoácidos. Por convención el orden
de escritura es siempre desde el grupo amino-terminal hasta el carboxilo final.
Para encontrar datos sobre las estructura de , por ejemplo la
hexoquinasa, navegue hasta Brookhaven
Protein Data Bank 3D browser y entre hexokinase
para la búsqueda, o SCOP
(Structural Classification of Proteins) y use la
referencia PDB número 1HKG.
|
|
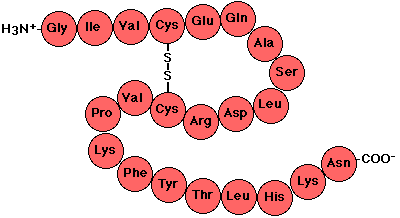
| Como consecuencia del establecimiento de enlaces peptídicos entre
los distintos AA que forman la proteína se origina una cadena
principal o "esqueleto" a partir del cual emergen las cadenas
laterales de los aminoácidos - |
|

|
| Estructura
primaria de la Insulina: consta de dos cadenas de AA enlazadas por
puentes disulfuro entre las cisteínas |
La estructura secundaria de una proteína es la que adopta
espacialmente. Existen ciertas estructuras repetitivas encontradas en las
proteínas que permiten clasificarlas en dos tipos: hélice
alfa y lámina beta.
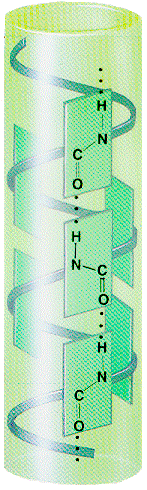
Una hélice alfa es una apretada hélice formada
por una cadena polipeptídica. La cadena polipetídica principal
forma la estructura central, y las cadenas laterales se extienden por fuera
de la hélice. El grupo carboxílo (CO) de un aminoácido
n se une por puente hidrógeno al grupo amino (NH) de otro
aminoácido que está tres residuos mas allá ( n
+ 4 ). De esta manera cada grupo CO y NH de la estructura central (columna
vertebral o "backbone") se encuentra unido por puente hidrógeno.
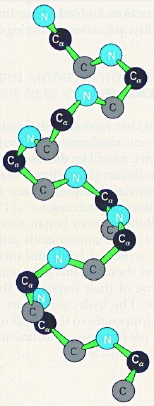
Existen tres modelos de alfa hélice. El primero
muestra solo al carbono alfa de cada aminoácido. El segundo
muestra todos los átomos que forman la columna vertebral del polipéptido
.
El tercero y mas completo modelo, muestra todos los puentes hidrógeno
que mantienen la alfa-hélice. Las hélices generalmente están formadas por aminoácidos
hidrófobos, en razón que son, generalmente, la máxima
atracción posible entre dichos aminoácidos. Las hélices se observan, en variada extensión, prácticamente
en todas las proteínas.
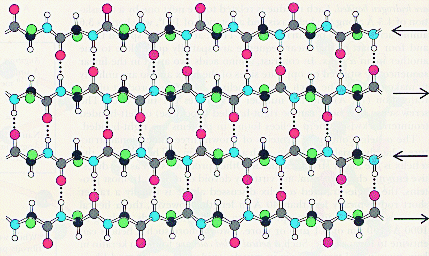
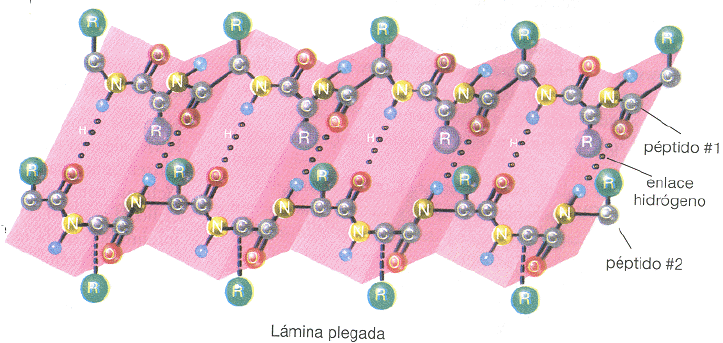
B-Las láminas beta son el otro tipo de estructura secundaria.
Pueden ser paralelas o antiparalelas. Las anti-paralelas generalmente se
ven así:
Y los giros que tienen en su estructura :
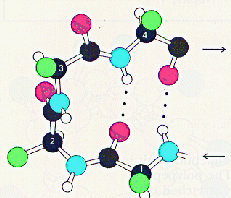
donde el aminoácido n se une por puente hidrógeno
al aminoácido (n +3) .
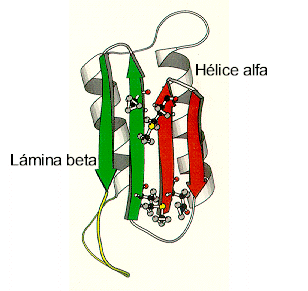
Existe un tipo especial de modelo molecular para resaltar la estructura
secundaria de las proteínas. Este tipo de modelo de proteína
representa los segmentos de lámina-beta como cintas en flecha (ribbons)
y las alfa hélices como como cintas en espiral.
|
|
|
Prión en su forma PrPsc presenta gran
proporción de láminas beta (43% láminas beta, 30% hélices alfa). |
El resto de la cadena
polipeptídica se referencia como un espiral al azar ("random
coil"), y se dibuja como una fina línea. Por favor, note que
espiral al azar o "random coil" es un nombre que lleva a confusión,
dado que las proteínas están altamente organizadas, pero
esta región no tiene una estructura secundaria con componentes difíciles
de categorizar.
La estructura terciaria es la estructura plegada y completa en
tres dimensiones de la cadena polipeptídica, la hexoquinasa que se
usa como icono en esta página es una estructura tridimensional completa.
A diferencia ded la estructura secundaria, la estrtuctura
terciaria de
la mayor parte de las proteínas es específica de cada molécula,
además, determina su función.
EL plegamiento terciario no es inmediato, primero se agrupan
conjuntos de estructuras denominadas dominios que luego se articulan
para formar la estructura terciaria definitiva. Este plegamiento está
facilitado por uniones denominadas puentes disulfuro, -S-S- que se
establecen entre los átomos de azufre del aminoácido cisteína.
Existen, sin embargo dos tipos de estructuras terciarias básicas:
-
proteínas
fibrosas, insolubles en agua, como la alfa queratina o el colágeno y
-
proteínas
globulares, solubles en agua.
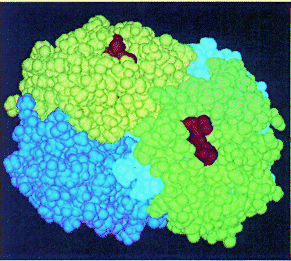
Solo está presente si hay mas de una cadena polipeptídica. Con varias
cadenas polipeptídicas, la estructura cuaternaria representa su
interconexión y organización. Esta es la imagen de la hemoglobina,
una proteína con cuatro polipéptidos, dos alfa-globinas y
dos beta globinas. En rojo se representa al grupo hem (complejo pegado
a la proteína que contiene hierro, y sirve para transportar oxígeno).
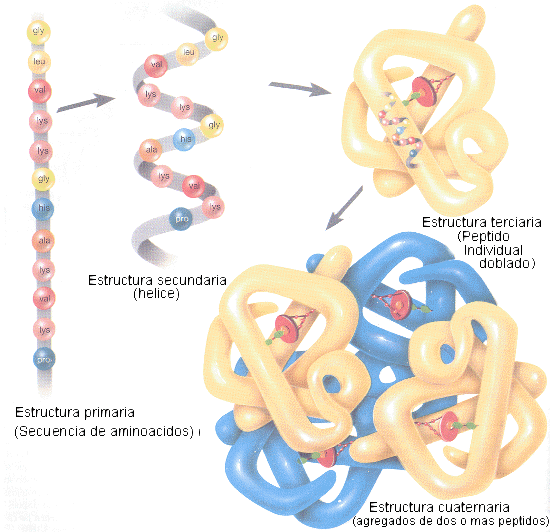
Los
cuatro niveles estructurales de la hemoglobina


[ Atrás ] [ Principal ] [ Arriba ] [ Siguiente ]
Traducción y diagramación a cargo de:
|