II. - El Polémico Agente Infeccioso
[ Principal ] [ Arriba ] [ Clasificación ] [ CRONOLOGÍA ] [ Prion Review: Chapter I (Introduction) ] [ El polémico agente ] [ Prion Review: Chapter III ] [ Prion Review: Chapter IV (PrP) ] [ Enfermedades por Priones ] [ ABREVIATURAS ] [ Referencias ] [ Prion Review: Chapter I (Introduction) ] [ Prion Review: Chapter II ] [ Prion Review: Chapter III ] [ Prion Review: Chapter IV (PrP) ] [ Prion Review: Chapter V (Prion Diseases) ] [ Tabla ]
-
II.1.- Descubrimiento de las Encefalopatías Transmisibles
La primera descripción de una encefalopatía de tipo espongiforme se
remonta al siglo XVIII, y hace referencia a la tembladera del carnero
(``scrapie'').
Las ovejas y cabras afectadas por la enfermedad sufren temblores y
fuertes pruritos. El análisis post-mortem del cerebro muestra
espongiosis, es decir, la presencia de vacuolas ópticamente vacias en el
tejido nervioso. A mediados del siglo XX dos investigadores de la
Escuela Veterinaria de Toulouse demostraron que el scrapie es una
enfermedad transmisible. Sin embargo, su hallazgo permaneció largo
tiempo en el olvido. Fue el pediatra americano C. Gajdusek quien
recuperó los resultados de J. Cuillé y P.L. Chelle, tras
percatarse de las similitudes clínicas y neuropatológicas entre el
scrapie y el kuru,
una enfermedad humana que en esa época estudiaba en Nueva Guinea. El
equipo de Gajdusek inoculó tejido cerebral de pacientes muertos
de kuru, por vía intracerebral, a chimpancés. Así, pudieron comprobar
que, efectivamente, tal como esperaban, el kuru también es transmisible.
A principios de los años 1920, Creutzfeldt y Jakob
describieron los primeros casos de una encefalopatía subaguda
espongiforme humana, que posteriormente recibió el nombre de enfermedad
de Creutzfeldt-Jakob (CJD) en
honor a sus descubridores. La CJD, que en un principio se había
clasificado como enfermedad degenerativa del sistema nervioso, también
resultó ser de carácter transmisible. El hecho se demostró en 1968.
Una vez descubierto el carácter infeccioso de las enfermedades, los
investigadores se lanzaron a la búsqueda del agente infeccioso.
Las encefalopatías subagudas espongiformes transmisibles (ESET)
causaron gran desconcierto entre la comunidad médica, por comprender
enfermedades de comportamiento y distribución muy diferentes. Así el 90%
de los casos de CJD son esporádicos, el kuru es de naturaleza infecciosa
y GSS
presenta un comportamiento genético clásico. En cuanto a la
distribución, el kuru es una enfermedad endémica de varias aldeas de
Nueva Guinea, mientras que scrapie presenta una amplia distribución.
El desconcierto fue en aumento a medida que salían a la luz las
peculiares propiedades del nuevo agente infeccioso. A nivel bioquímico,
se observó una insólita resistencia a diversos agentes desnaturalizantes
de ácidos nucleicos. Para mayor sorpresa, además, en el organismo
hospedador no se descubrieron los signos inflamatorios ni la respuesta
inmunitaria que generalmente se producen en enfermedades infecciosas.
-
II.2.- Hipótesis de los Virus Lentos no Convencionales
En los años 1960, varias enfermedades degenerativas del SN en
animales fueron atribuidas a infecciones víricas lentas. Estas
infecciones estan caracterizadas por periodos de incubación medibles en
años y un avance progresivo de los síntomas que conduce inevitablemente
hacia la muerte.
En 1966, Gajdusek puso de manifiesto que el
kuru,
en humanos, presenta a un esquema similar y afirmó que se trata de la
primera enfermedad por virus lentos identificada en el hombre. Poco
después diversas encefalopatías espongiformes fueron asimismo
clasificadas como enfermedades por virus lentos.
|
Encefalopatías Subagudas Espongiformes que en 1977 se
atribuían a Infecciones Víricas Lentas
|
|
-
En humanos:
-
En Animales:
|
|
Las infecciones víricas lentas supusieron el descubrimiento de un
nuevo agente infeccioso con unas propiedades físico-químicas y un
comportamiento biológico muy diferente del resto de los microorganismos.
En 1977, en un trabajo publicado en Science [19], Gajdusek
describe algunas de las propiedades no convencionales obtenidas a partir
de estudios del ``virus scrapie,'' transferido a ratones y hamsters.
Entre ellas destaca su inusual resistencia a varios agentes químicos y
físicos.
| Algunas Propiedades Físicas y Químicas de los Agentes
Infecciosos no Convencionales |
Propiedades Biológica |
- Resistencia a:
- Formaldehido
- EDTA
- Proteasas
(Tripsina, pepsina)
- Nucleasas (Ribonucleasas A y III,
Desoxiribonucleasa I)
- Calor (80°C)
- Radiación
ultravioleta (2540Å)
- Invisibles al microscopio electrónico
|
- Largo periodo de incubación (meses, años, decadas)
- No producen respuesta inflamatoria
- Patología crónica progresiva
- Fatal en todos los casos
- Carecen de estructuras visibles al microscopio electrónico
- No antigénicos
- Carecen de cuerpos de inclusión
- Presencia de ácido nucleico no
demostrada.
|
Debido a sus manifestaciones a nivel histológico, las enfermedades
atribuídas a virus lentos se clasificaron como encefalopatías víricas
subagudas espongiformes. La lesión neurohistológica básica en todas
ellas es una progresiva formación de vacuolas en dentritas, en axones y
cuerpos de neuronas. Otra característica distintiva de las infecciones
por virus lentos es la ausencia de respuesta inflamatoria en el cerebro.
Más aun, no hay evidencias de la existencia de respuesta inmune alguna
frente a los átipicos agentes infecciosos. Otra característica, que
desconcertó a los investigadores, fue la imposibidad de reconocer las
estructuras víricas en secciones de cerebro observadas al microscopio
electrónico.
Para Gajdusek y sus colaboradores la resistencia del agente
infeccioso de scrapie
a radiación ultravioleta de 254 nm no supuso una prueba de la no
existencia de información genética en forma de una molécula de ácido
nucleico, ya que los viroides demostraron una resistencia similar en
preparaciones crudas de plantas. Por otra parte, encontraron suficientes
propiedades víricas clásicas en los nuevos agentes infecciosos como para
seguir clasificándolos como virus.
|
Propiedades Clásicas de los Agentes
Infecciosos no
Convencionales |
- Filtrables con poros 25 nm o 100nm
- Periodo de adaptación a nuevos hospedadores
- Control genético de la susceptibilidad de algunas especies
- Existencia de distintas cepasA pesar de su excepcional
resistencia
a diversos agentes físicos y químicos, Gajdusek
encontró varias maneras para inactivar los supuestos virus
lentos. Por ejemplo,
aunque conservan su carácter infeccioso a temperaturas
superiores que los virus convencionales, observó
que
son rápidamente inactivados al sobrepasar los 85°C.
|
| Métodos de Inactivación |
- Autoclave 121°C
- Hipoclorito 0.5 - 5.0%
- Fenol 90%
- Eter
- Acetona
- Permanganato potásico 0.002M
- Urea 6M
- 2 - Cloroetanol
- Cloroformo
II.3.- Hipótesis de las Partículas Proteicas (Priones)
En vistas de la extraordinaria resistencia del agente infeccioso
de las ESET ante diversos tratamientos físicos y químicos, varios
investigadores comenzaron a poner en duda la intervención de un
virus lento. Ya en 1959, J.T. Stamp manifestó que le parecía
muy inverosímil que el factor infeccioso pudiera estar
constituido
por proteínas y ácidos nucleicos. Sin embargo, la firme
acceptación
del papel de los ácidos nucleicos en la replicación y el control
genético,
hizo que muchos investigadores no descartaran la existencia de
una partícula vírica, a pesar de que todos los experimentos
realizados hasta aquella fecha parecían apuntar a lo contrario.
Entre 1965 y 1966, Pattison y Field propusieron que
el agente
causante de scrapie reprentaba una nueva clase de partícula
replicativa. Field sugirió que podría tratarse de un
polisacárido y
que enzimas presentes en la célula hospedadoran podrían intervenir en
su replicación.
Alper et al. [1] estudiaron en 1967 el efecto de la
radiación
ultravioleta sobre suspensiones de extractos de cerebros
infectados de ratón. A partir de los resultados obtenidos
concluyeron que la replicación del agente causante de scrapie
no depende de un ácido nucleico. Observaron que el nivel
infeccioso del agente de scrapie no disminuye tras exposición
a una lámpara ultravioleta ``germicida'' estandar 15 W,
durante 1.5 h, a una distancia de 50 cm. En bacterias y virus,
el efecto de la luz ultravioleta sobre el proceso de replicación
depende de la longitud de onda, la cual suele corresponder con
el espectro de absorción de sus ácidos nucleicos.
Así, las longitudes de onda más efectivas oscilan entre 255 y 265 nm.
J.S. Griffith y R. Latarget fueron los primeros
investigadores que,
de forma independiente, propusieron que los pólemicos agentes
infecciosos podrían ser de naturaleza puramente proteica. La innovadora
hipótesis fue recibida con gran excepticismo por parte de la comunidad
científica.
Prusiner quedó intrigado por las ESET a raíz de la
muerte
de un paciente de CJD, cuando trabajaba como residente en
la Escuela de Medicina de la Universidad de California. Al revisar la
bibliografia, el artículo publicado por Alper en Nature
[1],
en el que éste y sus colaboradores proponían la existencia de
un nuevo tipo de partícula replicativa, acabó de atraer su
atención.
En 1974
Prusiner comenzó a trabajar para desvelar el misterio.
El primer paso fue la búsqueda de un método mecánico para purificar
el material infeccioso de los cerebros, para después poder analizar su
composición.
En 1982 su equipo consiguió aislar extractos puros del agente
infeccioso, a partir de cerebros de hamster.
Al igual que el equipo de
Alper, observaron que los métodos
que degradan ácidos nucleicos no reducen el nivel
infeccioso
de los extractos, y concluyeron que tanto DNA como
RNA están ausentes.
|
Métodos aplicados para dañar
ácidos
nucleicos |
- Nucleasas
- Psoralenos
- Hidroxilamina
- Iones Zn
- Radiación ionizante
- Radiación ultravioleta
| | |
Las mencionadas técnicas se aplicaron a homogenados
de cerebro, fracciones microsomales, preparaciones de
placas amiloides y complejos detergente-lípido-proteína. |
|
En vista de los resultados, Prusiner introdujo el término de
prion (``Proteinaceous infectious particle''), para
diferenciar el nuevo agente infeccioso de otros agente patógenos como
virus, viroides, bacterias, hongos o parásitos. Los priones fueron
definidos como partículas proteicas carentes de ácidos nucleicos.
Poco tiempo después se descubrió que los priones de scrapie contienen
una proteína hidrófoba proteasa-resistente de 27-30 kD, constituída por
una única cadena polipeptídica. Se la denominó proteína PrP
(``prion protein''). La proteína se acumula progresivamente en
los cerebros infectados durante el curso de la enfermedad. También se
identificaron placas amiloides compuestas por fragmentos de PrP.
Por otra parte se descubrió que los nivels de mRNA PrP son similares en
celebros de hamsters sanos e infectados por scrapie, por lo que el
acúmulo de PrP no puede deberse a un incremento en la velocidad de
síntesis de la proteína. El mecanismo de acumulación de PrP aún sigue
constituyendo una incógnita.
Con el hallazgo de PrP, surgió la pregunta de dónde se encuentra el
gen codificante para PrP (o gen PRP). La clave para resolver el
nuevo problema fue la identificación, en 1984, de unos 15 aminoácidos de
uno de los extremos de PrP. Dicha secuencia permitió a diversos
investigadores la construcción de sondas capaces de indicar la
localización exacta del gen PRP.
El gen fue finalmente hallado en el lugar que los partidarios de la
teoría del prion menos esperaban: en el genoma del hospedador. Mediante
pruebas diseñadas por el equipo de Hood, B. Oesch pudo demostrar
que las células de hamster contienen un gen PRP en su genoma.
Posteriormente se hallaron genes PRP en los cromosomas de todas las
especies susceptibles a contraer ESET. En el caso del hombre, en el
brazo corto del cromosoma 20. Una posible explicación era que el gen PRP
debía expresarse únicamente en los individuos afectados por las
enfermedades. Sin embargo, se pudo comprobar que PrP se encuentra
presente, de forma natural, en células de organismos sanos. Una primera
interpretación hizo pensar en una gran equivocación a la hora de
considerar la proteína PrP como el elemento esencial del carácter
infeccioso y patogénico de los priones. Pero, sorprendentemente, se
descubrió que la proteína PrP presente en los organismos sanos es
proteasa-sensible, mientras que la proteína PrP de los organismos
afectados por la enfermedad es proteasa-resistente.
La proteína PrP normal proteasa-sensible y la proteína PrP patogénica
proteasa-resistente, se denominaron PrPsen (o PrPc =
proteína celular) y PrPres (o PrPsc = proteína scrapie)
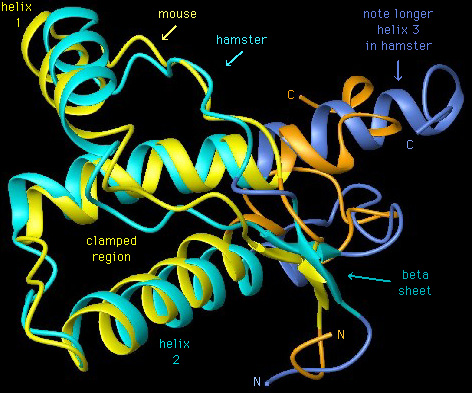
respectivamente. Análisis estructurales pusieron de manifiesto que la
proteína PrP celular posee una estructura en hélices alfa, mientras que
la proteína PrP anormal presenta mayor proporción de láminas beta. Ambas
proteínas son codificadas por el mismo gen y poseen idéntica secuencia
de aminácidos. Sin embargo, su conformación tridimensional es distinta,
en clara contradicción con el enunciado del Dogma Central de la
Biología de J. Monod: ``La secuencia de aminácidos
determina de manera unívoca la estructura terciaria de las cadenas
polipeptídicas.''
La existencia de los dos tipos de proteína PrP y el mecanismo que da
origen a la forma patogénica, así como la capacidad de PrPsc para
acumularse, constituyen el núcleo del debate actual. Según la teoría
de Prusiner, las PrPsc son capaces de inducir su estructura
espacial a las PrPc o a sus precursores, lo cual explicaría el
incremento de la concentración de PrPsc (Ampliado en el Capítulo
IV).
http://www-micro.msb.le.ac.uk/335/prionhms.jpg
|
|
-
II.4.- Hipótesis de las Moléculas Mixtas (Holopriones)
C. Weissmann, en un trabajo publicado en Nature[49] en
agosto de 1991, propone que el agente infeccioso esta compuesto por dos
componentes. Uno de los componentes es la proteína PrPsc (o
apoprion), capaz de causar enfermedades transmisibles incluso en
ausencia de ácidos nucleicos. El otro componente (o coprion)
contiene las propiedades fenotípicas que definen el linaje del agente
infeccioso (o holoprion). Se ha propuesto que el coprion es un
ácido nucleico (DNA o RNA), por ser transmisible y mutable.
Weissmann sugirió que los ácidos nucleicos que constituyen
copriones potenciales están normalmente asociados a PrPsc, pero que
también pueden estar presentes de manera independiente en las células de
individuos no infectados. Esta hipótesis implica que los copriones no
son esenciales para la patogénesis ni la propagación.
Según el modelo del holoprion, PrPsc sería capaz de propagarse por la
conversión de PrPc (o de precursores formados a partir de PrPc) en
copias de si misma, mediante modificaciones covalentes o cambios
conformacionales mediados por PrPsc o por el holoprion. Una vez que el
holoprion ha penetrado en una célula, su coprion puede ser replicado por
polimerasas celulares, proceso estimulado por la presencia de PrPsc. El
nivel de holopriones en el citoplasma crece a medida que las PrPsc de
nueva formación se van uniendo a los copriones sintetizados por las
polimerasas.
En la segunda parte de su modelo de propagación, Weissmann
intenta explicar por qué las preparaciones del agente infeccioso son
resistentes a nucleasas y a radiaciones. Weissmann afirma que el
carácter infeccioso y patogénico del holoprion radica en la proteína
PrPsc, de acuerdo con la propuesta de Prusiner y sus
colaboradores. Es decir, la destrucción del coprion no elimina el efecto
infeccioso de un extracto de tejido contaminado. Si una molécula de
PrPsc que ha perdido su coprion original penetra en una célula, puede
(pero no necesariamente) reclutar un ácido nucleico que le sirva como
coprion. El holoprion resultante posee propiedades fenotípicas que
difieren de las del holoprion original.
En 1994 Weissmann publica en Science [50] una
actualización de su modelo. En esta ocasión sugiere que en las células
neuronales normales, PrPc es transportada hasta la superficie celular,
de donde es endocitada y probablemente reciclada. Por infección de
PrPsc, las PrPc son convertidas en PrPsc en la superficie celular o en
el interior de las vesículas de endocitosis. La gran estabilidad de
PrPsc se presenta como el determinante de su acúmulo en la célula.
-
II.5.- Hipótesis Víricas
El hecho de que la hipótesis del prion no haya proporcionado
respuestas convincentes a muchas cuestiones básicas, ha llevado a
diversos investigadores a retomar la hipótesis del virus lento. Así,
para L. Manuelidis el argumento de que debe descartarse que el
agente infeccioso sea un virus, debido a su insólita resistencia a las
radiaciones ionizantes y ultravioletas, no es válido. De hecho, existen
virus conocidos que disponen de un sistema de reparación del material
genético que les permite resistir niveles de radiación similares. La
falta de respuesta inmune también puede ser justificada, ya que existen
virus lentos convencionales que escapan al sistema inmune instalándose
en el interior de las células.
La hipótesis vírica de Manuelidis no implica que PrP no
desempeñe un papel esencial en las enfermedades. Sin embargo, en este
caso se le atribuyen funciones distintas que en la hipótesis defendida
por Prusiner y sus colaboradores.
Manuelidis hace especial hincapie en varias características de
los agentes infecciosos, a saber:
- La existencia de distintas cepas
- Su multiplicación
exponencial
- Su tiempo de latencia prolongado
- Infección del
sistema retículo -endotelial (bazo, glóbulos blancos)
Como en
otras infecciones víricas, un cambio en un gen del hospedador
modificaría la capacidad del virus lento para infectarlo. Es decir, los
polimorfismos y las mutaciones del gen PRP podrían estar ligados a una
mayor susceptibilidad del hospedador frente a ciertas cepas del agente
infeccioso.
Para los partidarios de la hipótesis vírica, la epidemia BSE
constituyó una prueba a favor: al quedar sobradamente demostrada la
transmisión por vía oral, cabe preguntarse cómo resiste un agente
puramente proteico la acidez y el ataque de las enzimas en el aparato
digestivo. En cambio, muchos virus sí son capaces de sobrevivir a estas
condiciones. Manuelidis sugiere que, como el virus de la polio,
el agente infeccioso es transportado desde el intestino delgado por los
glóbulos blancos hasta el bazo, donde puede permanecer latente durante 5
a 20 años. Este razonamiento no es válido para un agente de naturaleza
puramente proteica.
Utilizando un nuevo método de purificación, H. Diringer halló
en 1994 lo que parecía ser la primera evidencia física de la existencia
de los virus. Su tamaño era inesperadamente pequeño: 10 a 20 nm. Ante la
dificultad de aislar las partículas víricas, Manuelidis argumenta
que una partícula provista de un ácido nucleico y proteínas de
protección puede no ser visible. Aproximadamente un año después, el
equipo de Manuelidis obtuvo un gel de electroforesis con bandas
que revelaban la existencia de RNA en extractos cerebrales de hamsters
con CJD.
Las bandas no pudieron localizarse ni en cerebros no infectados ni en
las librerias genómicas, por lo que fueron consideradas candidatas a
secuencias víricas. El tamaño de la partícula infecciosa fue evaluado en
unos 27 nm, tamaño similar al de varios virus conocidos. El genoma se
estimó en 1.000-3.000 pares de bases (retrovirus típicos: 10.000 pb;
virus de la hepatitis B: 3.500 pb; virus de la hepatitis C: 1.000 pb).
Los resultados publicados a mediados de 1995 por Manuelidis et
al. en Proc. Natl. Acad. Sci. USA [26], constatan que,
eliminando el 95% de la PrP de las partículas infecciosas de CJD con SDS
1%, éstas mantienen su carácter infeccioso. En cambio, su tratamiento
con Gdn-HCl 6 M, disminuye el nivel infeccioso en más del 99.5%. Los
investigadores concluyen que un ácido nucleico y una o varias proteínas
constituyen los componentes intrínsecos del virus CJD. Los dos
componentes no son infecciosos, a menos que se asocien en partículas
nucleasa-resistentes con un tamaño de 120S y un diámetro de unos 30 nm.
Los componentes parecen formar un complejo independiente de IAP, tal
como indica el hecho de que conserven su carácter infeccioso tras ser
sometidos a SDS 1%.
[ Atrás ] [ Siguiente ]
|
|