VIRUS ARN DE CADENA -VESteve Dewhurst, Associate Professor of Microbiology and
Immunology, University of Rochester Medical Center USA.
|
Sistema de complementación trans para el VSV-AG
|
La misma tecnología de
usar genomas del VSV con la glicoproteína-G borrada se ha usado para
estudiar las células huésped sensibles al virus Ebola. Por razones
obvias, los investigadores prefieren evitar trabajar con el virus Ebola
infeccioso.
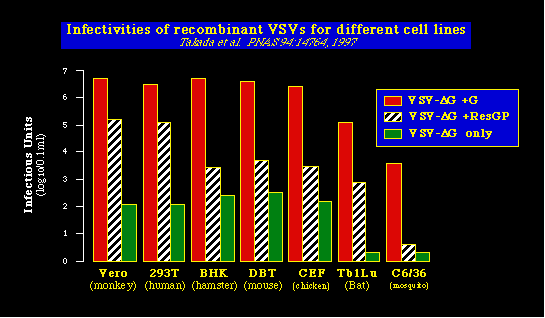
Note que éstos depósitos virales (VSV-DG +G) iniciales eran capaces solamente de un único ciclo infeccioso, ya que no pueden fabricar la proteína G por si mismos. Sin embargo en las células "transfectadas", los virus fueron capaces de adquirir la proteína G del VSV-G ó del virus Ebola (Ebo-GP), por el efecto trans. Entonces se examinó la infectividad y el rango de las células huésped susceptibles al virus VSV trans-complementado (ver más abajo). Los resultados demostraron que el Ebo-GP se une eficientemente a las células de los primates, pero es mucho más eficiente en la unión a las células de otras especies. |
Una variación en el procedimiento de la
complementación trans
en los VSV donde se ha borrado la proteína G, es el uso de una proteína G VSV
para generar pseudotipos del retrovirus. Los pseudotipos son el
resultado de una mezcla fenotípica de diferentes virus, contienen un núcleo (y
el genoma) de un virus, combinado con la envoltura (y su actividad de unión
ligada al receptor) de un segundo virus.
VSV-G Pseudotyped Retrovirus Vectors
Imágenes que son parte del excelente trabajo de M. Allende, N. Gaiano and N. Hopkins of MIT. Para mayor información, contacte Miguel Allende |
En líneas generales, los pseudotipos
pueden ser generados solamente entre virus estrechamente relacionados
(como el VSV y el virus Ebola), pero hay excepciones. Una de la más
notable son los retrovirus. Desde hace mucho tiempo se sabe que los VSV
pueden generar pseudotipos con una variedad de retrovirus, incluyendo al
HIV-1
|
Del mismo modo que pasa con el sistema VSV-DG,
los pseudotipos retrovirales pueden ser usados para estudiar las propiedades de
unión de la glicoproteína del virus Ebola a la membrana celular. Los
resultados de un estudio sobre este tema se muestran más abajo. En este caso,
los investigadores generaron pseudotipos retrovirales que llevaban
glicoproteínas en la envoltura que procedían ya de otro retrovirus que tiene
un mayor alcance de unión a distintas células huésped (AmphoEnv) ó
procedían del virus Ebola (EbolaGP). Em ambos casos, ellos empaquetaron
el genoma de un retrovirus recombinante que contenía el gen luciferasa de la
luciérnaga. Esto les permitió valorar con facilidad el grado de infectividad
de los pseudotipos retrovirales para diferentes líneas celulares, midiendo la
producción de luciferasa por medio de un método basado en la luminiscencia.
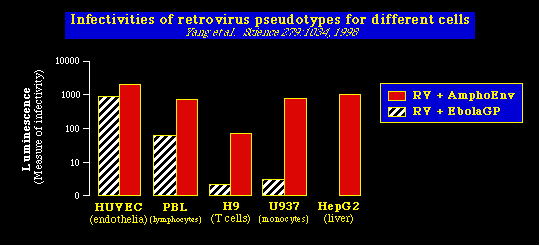
Tal y como se muestra más abajo, éstos experimentos revelaron que la
glicoproteína del virus Ebola interacciona eficientemente con un receptor que
está presente en las células endoteliales vasculares de la especie humana
(HUVECs), pero la glicoproteína es menos eficiente, cuando interacciona con
moléculas de superficie de otras células humanas como las células T, los
monocitos y células hepáticas.
PARAMYXOVIRIDAE
Referencias: Lamb and Kolakofsky, Fields Virology, 3rd Ed., Chapter 40
(Paramyxoviridae)
Griffin and Bellini, Fields Virology, 3rd Ed., Chapter 43 (Measles virus)
IMMUNE EVASION BY MV: Bhardwaj, N. J. Exp. Med. 186:795, 1997
Taxonomía
Subfamilia Paramyxo- virinae (Género: Paramyxo-, Morbilli-, Rubula-)
- Paramyxo-: eg, Parainfluenza viruses 1 and 3: tienen H y N (una sola molécula: HN)
- Rubula-: eg, virus de las papaeras: tienen H y N (una sola molécula: HN); tiene un gen extra (SH)
- Morbilli-: eg, virus del sarampión: tiene el H y le falta el N
Subfamilia: Pneumo- virinae (Genus: Pneumovirus)
- neumo-: eg, virus respiratory syncitial (RSV): le falta el H y el N; es más divergente.
Biología Molecular
NOTA: las proteínas C, V son codificadas desde secuencias de lectura que se superponen
dentro de la región de los genes P.
Virus del sarampión: Proteínas de la Ribonucleoproteína (RNP)
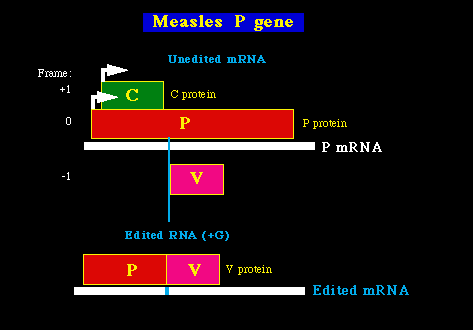
Las Ribonucleoproteínas del virus del sarampión incluyen la Polimerasa, Nucleoproteínas y Fosfoproteínas, las cuales son más ó menos equivalentes a su homólogas en los rhabdovirus. Una diferencia importante entre estas dos familias virales es que los genes P del virus del sarampión codifican dos proteínas más, ademas de la fosfoproteína. Estas dos proteínas extra son codificadas por el mRNA de los genes P, pero son traducidas usando diferentes codones de iniciación de metionina y secuencias de lectura superpuestas. El primero de estas proteínas es la proteína C, la cual es una proteína básica pequeña producida desde una plantilla de lectura abierta (open reading frame (ORF) ) que se superpone al N-terminus de la región de los genes P, en la secuencia +1. La proteína C es codificada a partir de las transcripciones de los genes P por medio de una iniciación interna translacional. Debe resaltarse que, en una proporción molar, la proteína C es el mayor producto de los genes P en muchos de los paramixovirus, y varias formas de la proteína C pueden ser producidas en algunos virus, debido al empleo de algunos codones de iniciación de methionina. La función de la proteína C parece ser la de ayudar a regular los cambios entre la transcripción mRNA y la replicación viral. De modo específico, la proteína C inhibe la síntesis de mRNA, pero tiene un efecto mínimo en la replicación del genoma.
La segunda proteína de los genes P es la proteína V. El mRNA de los genes P del virus del sarampión es editado de modo co-transcripcional en un lugar específico situado en la parte final del C ORF. Este evento de edición del ARN comprende la adición de un residuo G no secuenciado en ésta posición durante la síntesis del mRNA. (Ocurre porque la ARN polimerasa "tartamudea" cuando encuentra una cadena de residuos C en la plantilla de la cadena del ARN; por qué ocurre en este lugar y no en otro puede estar en relación con la estructura del ARN). El resultado de la adición de este residuo G extra al mRNA, es que después de la translación, la mitad del N-terminal de las secuencias de la proteína P no pueden ser unidas a la parte normal C-terminus, pero si lo hacen a una región acidófila rica en cistina de la proteína V de la ORF (la cual está en -1 ORF en relación a P). La proteína formada de este modo se la conoce como proteína V y su función no es bien conocida, aunque hay evidencia que sugiere que su acción es la de inhibir la replicación del genoma, sin actuar sobre la transcripción del mRNA.
¿ Cuál es la causa de la complejidad del gen P ? Probablemente no es la de ahorrar espacio, ya que el genoma es grande y puede codificar otras pequeñas proteínas. Lo más probable es que es un modo de co-expresar proteínas, las cuales pueden interaccionar ó funcionar en un punto común en el proceso de la replicación
Virus del sarampión (VSa): Proteína Matrix (M).
Es una proteína que funciona de modo parecido a su homóloga en los rhabdovirus. La proteína M es básica (en un pH neutro tiene una carga neta+) y muy abundante en los viriones. Se cree que la proteína M es el organizador central en la morfogénesis viral, y puede interaccionar tanto con sí misma y con la nucleocápside viral como con los C-terminales (anclas de la transmembrana) de las proteínas F y H. La proteína M es por eso importante para la extrusión viral de la célula y para la infectividad viral, y el gen M está frecuentemente defectuoso (mutado) en las infecciones persistentes por el VSa , donde la extrusión viral no ocurre, como es el SSPE (subacute sclerosing pancephalitis), encefalitis esclerosante subaguda, un síndrome raro y fatal, en el cual existe una infección por el VSa persistente en el cerebro.
Virus del sarampión: proteínas de la envoltura.
Todos los paramyxoviridae poseen 2 membranas ó proteínas que lo envuelven. Una está relacionada con la fijación a la célula y la otra con la fusión a la membrana de la célula huésped, independiente del pH.
Proteína de fijación: estas proteínas se unen a los receptores celulares que contienen ácido siálico y por eso estos virus son capaces de aglutinar los hematíes (hemaglutinación). En el caso de los paramyxovirus y rubulavirus, las hemaglutininas virales tienen también actividad de neurominidasa, y por eso se las conocen como proteínas HN (hemaglutinina-neurominidasa). En el caso de los virus morbillivirus, sus hemaglutininas no tienen actividad neurominidasa. Por eso el virus del sarampión codifica una proteína H y no la proteína NH.
Función de la Neurominidasa: Se cree que previene la agregación de las partículas virales a la membrana de la célula huésped durante la extrusión de los viriones de la célula, facilitando de este modo la liberación de las partículas virales de la célula infectada. Lo que significa que la neurominidasa debe de ser neutralizada en la fase inicial de la entrada viral y debe de activarse en la fase tardía cuando empiezan a liberarse los viriones. En parte ocurre porque las actividades de la hemaglutinina y de la neurominidasa están reguladas por el pH y por la concentración de los iones haluro (compuestos binarios formados por la combinación de un halógeno con un elemento ó radical más electropositivo). Específicamente, el pH y la concentración de iones haluro del espacio extracelular es ideal para la hemaglutinación, mientras que la neurominidasa actúa mejor en medio ácido, como el que se puede encontrar en el aparato de Golgi del medio intracelular.
El virus del sarampión (VSa) no usa el ácido siálico como su receptor, posiblemente porque su proteína H tiene una afinidad muy baja para el ácido siálico. Por eso el VSa no necesita la neurominidasa. La proteína H del virus del VSa se une a un receptor específico, CD46, una molécula que es un miembro de la superfamilia de los genes de la inmunoglobulinas, y sirve como como un receptor celular para los componentes del complemento C3b y C4b. Este receptor está distribuído ampliamente en los tejidos humanos y se expresa relativamente a niveles bajos, lo cual significa que es poco probable que pueda causar agregación viral durante la extrusión e los viriones.
Los neumovirus y el virus respiratorio syncitial (RSV = respiratory syncytial virus) no hemaglutinan y se desconoce su receptor. En estos casos la fijación de los virus a la membrana celular se hace por medio de la glicoproteína G.
Proteína de fusión (F): Las
proteínas de fusión de los paramyxovirus, están hechas inicialmente a partir
de un precursor inactivo (F0). Este es fragmentado por las proteasas
celulares para producir un fragmento N-terminal (F2 ) y un fragmento
más largo C-terminal (F1). estos dos fragmentos permanecen unidos
por un puente disulfuro. El proceso de proteolisis expone una región
hidrofóbica y fuso-trópica en el N-terminus del F1. Recalcar que el proceso proteolítico que sufre la proteína
es esencial para la infectividad viral, ya que las células que no pueden procesar F, no
son susceptibles de ser infectadas.
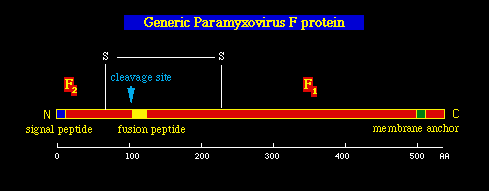
La región altamente hidrofóbica de la proteína F está muy protegida del espacio acuoso que la rodea, ya que el contacto con el agua podría resultar en una agregación de la proteína. Presumiblemente, hay un cambio de conducta durante la infección viral en el que se produce una exposición de la zona de fusión, de un modo similar al descrito para el virus de la influenza. Hay sin embargo una diferencia, y es que los paramyxoviridae inducen una fusión a un pH neutro, mientras que los virus de la influenza requieren un pH ácido endosómico. De este modo los paramyxoviridae pueden inducir una fusión desde fuera. Los viriones pueden inducir una fusión rápida de las células (antes de la replicación viral) cuando se añaden a los cultivos celulares en altas concentraciones. Por eso las envolturas de los virus Sendai ó partículas virales inactivadas de los virus Sendai se han usado por años para promover fusiones celulares y obtener híbridos (como los que se usan para la producción monoclonal de anticuerpos).
Otras proteínas de la envoltura. Los rubulavirus contienen un gen pequeño llamado SH (short hydrophobic protein= proteína corta hidrofóbica) localizada entre F y HN. Es una proteína integral de la membrana cuya función se desconoce. Los neumovirus también codifican la proteína SH
Características únicas de los pneumovirinae

Proteínas no estructurales, NS1 y NS2.
Los neumovirinae codifican dos proteínas cortas, no estructurales, muy
abundantes. Se desconoce su función.
Proteína SH . Tmbién se encuentra en los rubulaviruses.
Proteína 22K (sinónimo: Proteína M2). El gen que codifica esta
proteína se encuentra entre los genes F y L.
Productos del gen P . No se producen las proteínas C y V
Además, la organización del genoma de los neumovirus es única por:
- El orden de los genes G y F está invertido (El M2 está adyacente al L).
- Más importante, los genes M2 (22K) y L se superponen por 68 nts.Así, no existe una secuencia intergénica contracorriente de L y de ese modo la única manera de producir la proteína L es ignorar la señal de finalización de la transcripción que está al final del gen M2 (22k). El resultado es disminuir la expresión del gen L
Replicación de los Paramyxovirus
En términos generales la replicación de los paramyxovirus es bastante similar a la de los rhabdoviruses.
Una característica única e importante de la infección por el virus del sarampión es su habilidad para infectar de modo persistente las células cerebrales, mecanismo implicado en el SSPE La infección crónica por el VSa parece incluir al menos dos vías para una atenuación específica de la expresión del gen M. Primero, una regulación a la baja de la expresión del gen M como resultado de una finalización transcripcional ineficiente y una poliadenilación en el ORF que está contracorriente (el cual es expresado con normalidad). Segundo, se ha descrito una hipermutación condicionada de la región del gen M Lo que parece ser debido a la acción de un enzima celular que convierte las adenosinas a inosinas en el dsRNA (double-stranded-ARN-adenosine deaminase, dsRAD = ARN bicatenario Adenosín Deaminasa, dsRAD). Fíjese en que el dsRAD es también responsable para la edición específica de lugar del ARN del virus de la Hepatitis delta !
Otra característica importante de la replicación de los paramyxovirus es la gran diversidad de la expresión del gen P. Esto se debe tanto a la variedad de posibilidades translacionales (seleccionar cuál codón ATG será usado para iniciar la síntesis de proteína, ya sea la P ó la C) y también a la variedad transcripcional (como la inserción de cualquier residuo G en la región P del mRNA, lo que permite la expresión de la proteína V).
Patogénesis de la infección por el virus del sarampión
El virus del sarampión (VSa) es un patógeno clásico emergente. El VSa es relativamente una nueva infección para los humanos, evolucionó de un morbillivirus animal (El VSa se parece mucho a un patógeno del ganado vacuno conocido como el virus rinderpest). Se describión el sarampión por primera vez en el siglo X. Debido a que causa una infección aguda muy contagiosa que produce inmunidad de por vida, no tiene un reservorio animal y requiere un habitat urbano para sobrevivir (por encima de 200,000 personas). Las primeras ciudades con este tamaño aparecieron hace unos 3.000 años en Egitpo y Samaria. Y posiblemente fué cuando apareció el sarampión y las paperas. Estas ciudades permaneciern aisladas hasta que floreció el comercio. Y las epidemias (sarampión, viruela) empezaron hacia los 200-400 AD. El sarampión fué llevado al Nuevo Mundo por los Europeos y causaron miles de muertes entre los nativos de America.
Un ejemplo reciente de una infección emergente por morbilliviru ocurrió en Australia en 1994. 14 caballos murieron por una infección por morbillivirus equino (EMV = equine morbillivirus) en Queensland. Dos personas que estaban en contacto con estos caballos se infectaron y uno de ellos desarrolló una severa enfermedad respiratoria. Un segundo caso fatal de infección por EMV fué descrito a 800 km de la primera zona. Estudios subsiguientes han revelado que la infección del EMV de los caballos es muy rara. Sin embargo el virus se ha hallado en los murciélagos, sugiriendo que estos animales pueden ser el reservorio natural de estos virus.
El VSa es el mayor asesino de los niños del mundo. A nivel mundial, el VSa mata un millón de niños cada año de acuerdo con la OMS. El tamaño del problema se ha visto más claro después de que se ha hecho un esfuerzo gigantesco para vacunar cerca del 80% de los niños en la campaña de vacunación entre 19980 y 199o. Si este esfuerzo, el sarampión hubiera matado 3 millones de niños por año.
A pesar de todo, la OMS y la UNICEF, trabajan denodadamente para aumentar los porcentajes de niños vacunados en las aldeas, pueblos y ciudades, incluyendo las áreas mas desfavorecidas, y para desarrollar vacunas anti-sarampión más eficaces en los niños menores de dos años. Esto es muy importante, ya que la infección es más severa en esa edad y son los que tienen más riesgo en las naciones en vías de desarrollo.
En las naciones industrializadas, las epidemias por el VSa surgen a pesar de la vacunación. Por ejemplo, en US apareció una epidemia entre 1989 y 1991 que produjo 55,000 enfermos y cerca de 130 muertes. Se achacó la epidemia al hecho de que el % de vacunación infantil en los niños pre-escolares en las áreas más pobladas de las ciudades, estaba por debajo del 50%.
Ultimamente la OMS y la UNICEF intentan erradicar el sarampión completamente. Es posible por varias razones: 1) no existe un reservorio animal, 2) solo hay un serotipo viral, 3) la mayoría de los casos se diagnostican clínicamente y 4) hay una vacuna efectiva disponible. (Una vacuna hecha de virus vivos atenuados que se administra a los 9 meses en las áreas donde el virus permanece prevalente y a los 15 meses en las demás partes; en USA se administra como parte de la vacunación MMR):
Patogénesis: El sarampión es una infección de la infancia que se propaga por vía respiratoria.Después de la infección, el virus se reproduce en el tejido linfático, después entra en la corriente sanguínea (fase de viremia) y se propaga al resto del cuerpo llegando a los órganos diana (principalmente los pulmones) donde se reproduce otra vez. El período de incubación es de 10-14 días y es asintomático y al final del cual empieza a ser evidnete la enfermedad con: conjuntivitis, tos y fiebre. A los 2-3 días del inicio de los síntomas aparece la erupción cutánea característica de la enfermedad, que coincide con la aparición de la respuesta inmune. La convalescencia va acompañada con una inmunidad a la infección para toda la vida.
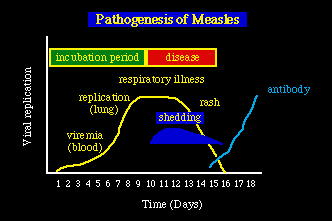
Respuestas immunes. La recuperación del sarampión está mediada en
parte por una respuesta inmunitaria celular al virus (células T citotóxicas,
CTLs). Una de las características más interesantes del VSa es su habilidad
para producir una supresión de la inmunidad in vivo
y en in vitro. La producción de respuestas celulares a nuevos
antígenos está bastante inhibida, lo que predispone al niño infectado por el
VSa a infecciones oportunistas por otros patógenos. (como bacterias, las cuales
pueden causar una neumonía de curso fatal)
Se cree que el mecanismo por el cual el VSa produce una supresión de la respuesta inmune es la infección de las células dendríticas DC (dendritic cells, las cuales son responsables de la presentación del antígeno) y de otras células del sistema inmunitario. La infección de las células dendríticas por el VSa lleva a la apoptosis y a la inhibición de las DC para estimular la proliferación de las células T (que son una parte esencial para la elaboración de la respuesta inmune). Hay también una inhibicion de la interleucina (IL)-12 producida por los monocitos. Este fenómeno parece que ocurre, en parte, por la acción de enlaces cruzados mediados por el virus, en el receptor CD46 (Karp et al., Science 273:228, 1996). El IL-12 es crucial para el desarrollo de una respuesta Thl (requerida para la generación de respuestas mediadas por células, las cuales proveen la línea primaria de defensa en contra de las infecciones virales).
Autoinmunidad. Además de la supresión de la respuesta inmune, la infección del sarampión puede estar asociada con autoinmunidad. De moso específico, una enfermedad desmielinizante autoinmune, la encefalomielitis post-infecciosa (EPI) es una complicación importante que aparece a los 14-28 días de la infección con una incidencia de 1 en 1000 casos. Se asocia a una respuesta inmune en contra de una proteína básica de la mielina. No está claro cómo se inicia este proceso, aunque es posible que los antígenos del VSa puedan imitar a la mielina (imitación molecular). De este modo la respuesta inmune anti-VSa puede atacar a un atígeno propio: la mielina.
PANEL izquierdo: LPS = lipopolisacárido; un activator eficiente de monocitos
anti-CD46: anticuerpos al CD46 (enlaces cruzados)- PANEL derecho: DC: células dendríticas Normalmente, las DC estimulan la proliferation células T allogénicas; no lo hacen si son infectadas por el VSa
Infección persistent. El VSa puede establecer una infección crónica in vivo y en in vitro. Tal y como se mencionó antes, esta infección se asocia con la supresión de la expresión de la proteína M viral. Se puede asociar con una enfemedad muy rara, la Pan Encefalitis Subaguda Esclerosante PESE (SSPE =Subacute Sclerosing PanEncephalitis) que peuede aparecer muchos años después de la primoinfección y afecta a 1 de cada 1.000.000 de niños.
Características clínicas y complicaciones del sarampión: los síntomas más serios incluyen:
- Enfermedad respiratoria. La neumonía puede ser producida por el mismo virus VSa (neumonía de células gigantes), principalmente en personas inmunodeprimidas ó de modo más habitual por bacterias oportunistas, hecho más frecuente.
- Enfermedad gastrointestinal. La diarrea es una complicación muy común. Puede ser un grave problema en niños malnutridos. La severidad de la infección es peor en niños con deficiencia en vitamina A. Es una de las razones por las cuales la OMS y la UNICEF apoyan los programas con suplementos de vitamina A en el mundo en vías de desarrollo (la vitamina A se puede administrar en cápsulas de modo muy barato y en grandes dosis
- Enfermedad neurológica. La Encefalopatía Post Infecciosa (EPI) afecta a 1 de cada 1000 infectados, usualmente dentro de los siguientes 14-28 días de la infección. En las personas inmunocomprometidas la enfermedad progresa lentamente (encefalitis con cuerpos de inclusión del sarampión), y la PESE afecta en un porcentaje muy bajo a los niños normales, usualmente años después de la primoinfección.
- Enfermedad Ocular. El virus del sarampión (VSa) es una causa importante de ceguera de bido a la aparición de lesiones corneales. De nuevo la deficiencia de vitamina A ha sido implicada en la ceguera y la deficiencia en Vitamina A puede aumentar el daño ocular inducido por el virus.
- Sarampión atípico. Se ha visto una forma severa de sarampión, con mayor postracción, fiebre más prolongada, lesiones dérmicas más pronunciadas en personas que recibieron la vacuna del sarampión inactivada usada en USA entre los años 1963-1967. esta vacuna inactivada por formol, provocó una respuesta inmune desbalanceada, con niveles altos de anticuerpos a la proteína H viral pero con escasa reactividad a las prpteínas virales F ó N.
Otros paramyxovirus
Virus respiratory syncitial (RSV). El RSV infecta a los niños desde las 6 semanas hasta los 6 meses de edad, causa 90.000 hospitalizaciones y 4500 muertes cada año en USA, Poduce una infección de las vías respiratorias altas y en un 25-40% de los casos complicaciones de las vías respiratorias bajas. El RSV es la causa viral más importante de las infecciones del tracto inferior de las vías respiratorias en bebés y niños. En las personas mayores, puede aparecer una neumonía severa. El RSV es la causa más frecuente de las infecciones nosocomiales (de los hospitales). Puede serúitil la ribavirina en aerosoles, como tamnién administrarle anticuerpos pasivos (inmunoglobulina anti-RSV). existen dos subtipos, pero no existe una vacuna efectiva, en parte porque: 1) la reinfección es muy común, y 2) la inmunidad es incompleta. (la infección ataca a los lactantes a pesar de la presencia de los anticuerpos maternos).
Virus de la paraInfluenza PIV-1, 2 y 3 son la segunda causa, después del RSV, de infecciones graves del tracto respiratorio en los lactantes y niños.
Virus de las paperas. las paperas producen una enfermedad sistémica febril con inflamación de las glándulas salivales. Puede infectar al sistema nervioso y producir meningitis, encefalitis, sordera y orquitis. Una vacuna atenuada con virus vivos se ha usado en USA desde 1967, las paperas es ahora una enfermedad rara en USA.
Actualizado el 1/99, Steve
Dewhurst, Associate Professor of Microbiology and Immunology
© Copyright University of Rochester and Stephen Dewhurst, 1996-99
URL: http://www.urmc.rochester.edu/smd/mbi/grad2/nns99B.html
![zebra1sml[1].gif (31554 bytes)](images/zebra1sml1.gif)